烯烃的臭氧化、炔烃的氧化
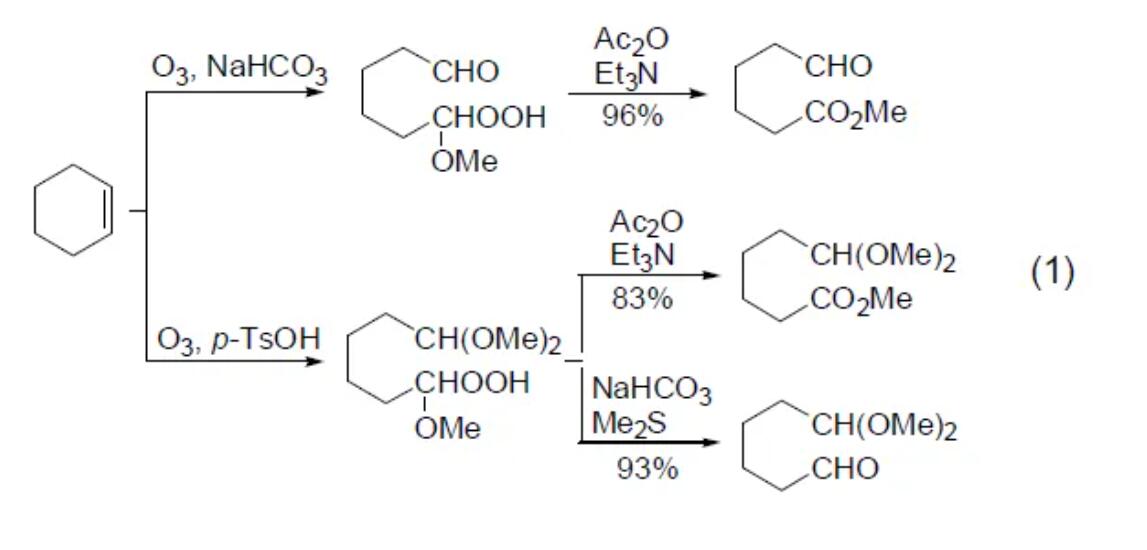
臭氧广泛的用途是进行碳碳双键的氧化断裂,根据后处理条件的不同可生成羰基化合物或醇。这些反应一般是在低温(–25~–78 oC)下,混合于空气或者氧气中的臭氧气流通过底物在惰性溶剂中进行的。常用的溶剂是CH2Cl2和MeOH,或者是二者的混合溶剂。很多烯烃都能进行臭氧化反应,给电子基团取代的双键比吸电子基团取代的双键反应更快。还原的后处理过程生成醛、酮或者醇。用LiAlH4或NaBH4后处理可以全部还原为醇。氧化的后处理过程把过酸的臭氧分解产物转化为酮或者羧酸[1]。用该方法可以从环烯出发制备许多产物 (式1)[2]。
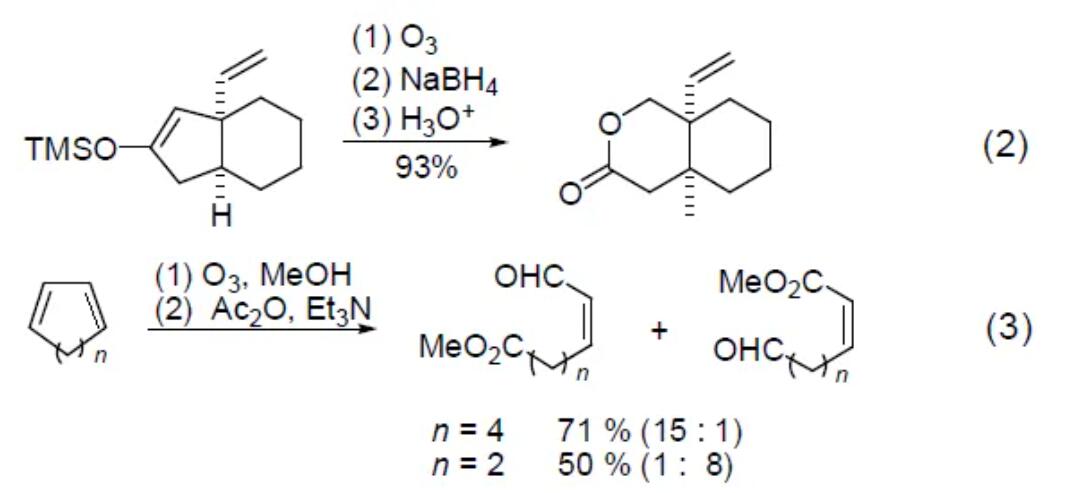
三甲基硅氧基烯由臭氧氧化断裂,再经过氧化后处理过程生成二酸,或者经过还原后处理过程生成羟基或含氧衍生物 (式2)[3]。如果后处理条件恰当,这个反应就是Baeyer-Villiger氧化的一个很好的补充。α,β-不饱和酮与臭氧的反应一般得到比原分子少一个碳的酮酸。1,3-二烯的臭氧分解反应中,双键能够发生选择性的氧化断裂,在1,3-环二烯中,一级臭氧化物碎裂的区域选择性取决于环的大小 (式3)[4]。位阻大的烯用臭氧化处理一般生成环氧化物。
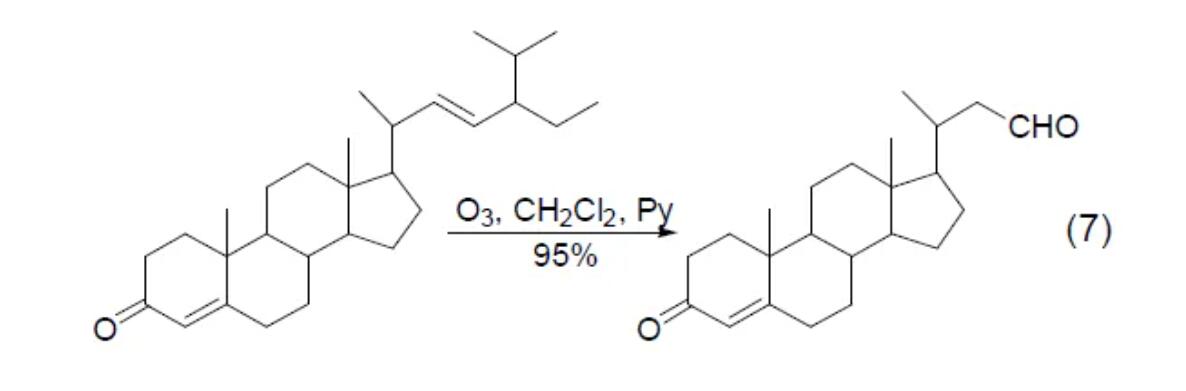
加入 Lewis 酸可以增强臭氧的亲电反应性。相反的,在臭氧化反应中加入少量吡啶,可以明显降低臭氧的反应性而同时提高臭氧进攻的区域选择性 (式7)[8]。
相对于其它烯烃的氧化断裂试剂而言,臭氧是比较好的一种。其它试剂如四氧化锇、高锰酸钾、高碘酸钠或羧酸镉等都价格昂贵、有很高的毒性,并且会造成金属离子污染,后处理步骤复杂。
炔烃的氧化
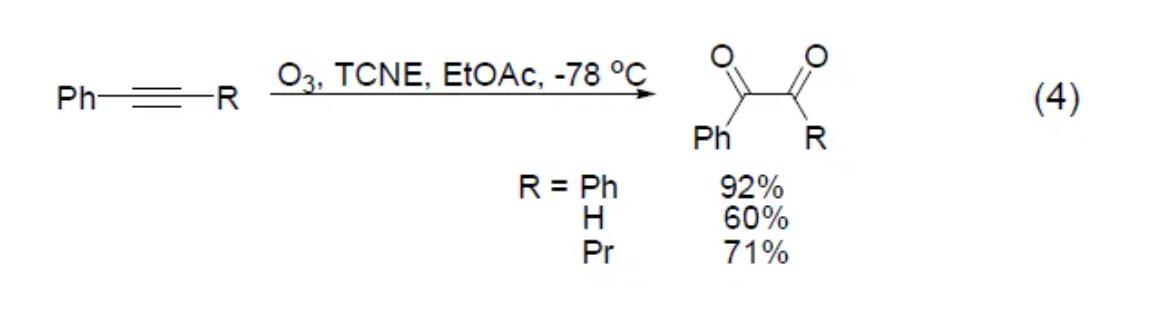
炔烃与臭氧的反应比烯烃与臭氧的反应慢[5]。当同时有烯键和炔键存在时,烯键会优先发生反应。炔烃与臭氧反应既可以产生羧酸,又可以产生α-二羰基化合物(还原后处理过程) (式4)[1]。很多还原试剂都可以用来生成α-二羰基化合物。端炔在臭氧作用下能够得到α-羰基醛。
芳香体系的臭氧分解
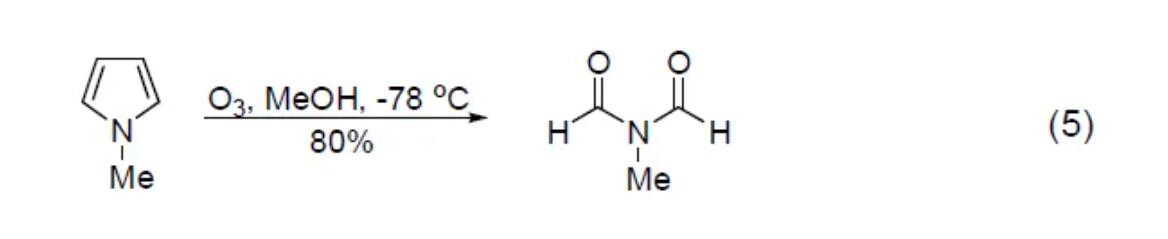
芳香化合物对臭氧的反应性比烯烃和炔烃弱。杂环体系的臭氧分解反应主要包括从喹啉合成吡啶衍生物,臭氧分解咪吡咯得到N-乙酰氨基化合物 (式5)[6],臭氧分解呋喃体系释放出潜在的羧酸官能团等。
杂原子的臭氧化
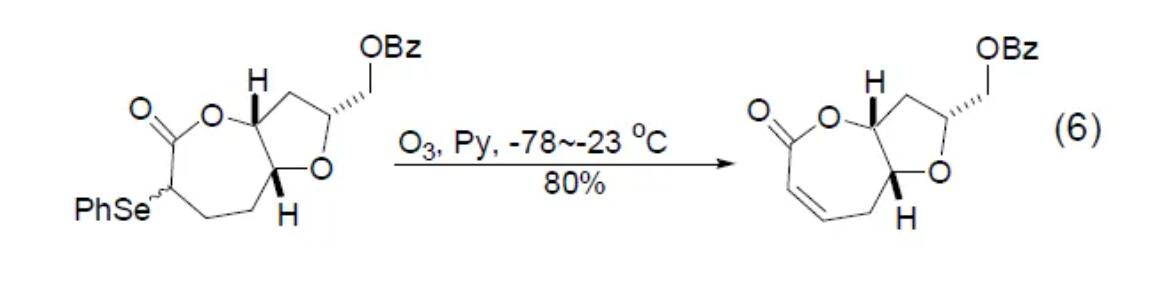
在臭氧作用下,磷化氢可以转化为氧化膦,亚磷酸盐可以转化为磷酸盐。有机硫化物在臭氧作用下可以转化为亚砜或者砜。三级胺臭氧化可以转化为氧化胺,而一级胺臭氧化则以适中产率生成硝基化合物。硒化物在臭氧作用下转化为硒氧化物,此反应经常用于制备不饱和羰基化合物 (式6)[7]。
其他
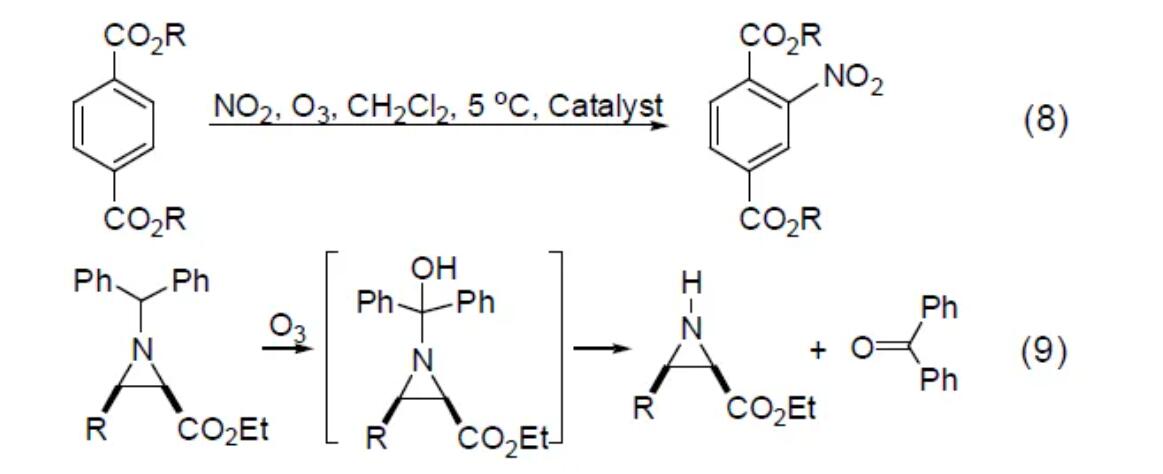
醛可以通过在乙酸甲酯或乙酸乙酯中臭氧化转化为过酸,或者在10% 的KOH甲醇溶液中臭氧化得到甲酯。在催化剂量的Fe3+存在下,在臭氧作用下,NO2可以直接将苯二甲酸酯硝化 (式8)[9]。臭氧还可以氧化氮杂环丙基酯上的N-二苯甲基保护基团,得到脱保护的氧化氮杂环丙基酯和二苯甲酮 (式9)[10]。
参考文献
1. (a) Razumovskii, S. D.; Zaikov, G. E. Ozone and Its Reactionswith Organic Compouds, Elsevier: Amsterdam, 1984. (b)Hudlicky, M. Oxidation in Organic Chemistry, AmericanChemical Society: Washington, 1990.
2. Gupta, D.; Soman, R.; Dev, S. K. Tetrahedron, 1982, 38,3013.
3. (a) Clark, R. D.; Heathcock, C. H. Tetrahedron Lett., 1974,2027. (b) Clark, R. D.; Heathcock, C. H. J. Org. Chem., 1976,41, 1396.
4. Wang, Z.; Zvlichovsky, G. Tetrahedron Lett., 1990, 31, 5579.
5. Dieter Cremer, D.; Crehuet, R.; Anglada, J. J. Am. Chem. Soc.,2001, 123, 6127.
6. Kashima, C.; Harada, K.; Hosomi, A. Heterocycles, 1992, 33,385.
7. Grese, T. A.; Hutchinson, K. D.; Overman, L. E. J. Org.Chem., 1993, 58, 2468.
8. Haag, T.; Luu, B.; Hetru, C. J. Chem. Soc., Perkin. Trans. I,1988, 2353.
9. Nose, M.; Suzuki, H.; Suzuki, H. J. Org. Chem., 2001, 66,4356.
10. Patwardhan, A. P.; Lu, Z. J.; Pulgam, V. R.; Wulff. W. D.Org. Lett., 2005, 7, 2201.
本文转自:《现代有机合成试剂——性质、制备和反应》,胡跃飞等编著